Non capita spesso in una conferenza scientifica di assistere, anzi partecipare, a ripetute “standing ovation” quasi che sul palco ci fossero rockstar e non ricercatori. Eppure è quanto successo alla XVIII Conferenza Internazionale sull’AIDS tenutasi a Vienna dal 18 al 23 luglio quest’anno – oltre 20.000 partecipanti - quando sono stati presentati i risultati dello studio clinico di fase III (efficacia clinica) “CAPRISA 004”.
Lo studio aveva lo scopo di dire l’ultima parola sulla potenziale efficacia di un gel vaginale contenente 1% di Tenofovir (un inibitore dell’enzima retrotrascrittasi di HIV, ma anche del virus dell’epatite B). In contrasto con l’euforia che la notizia diffondeva tra i partecipanti il quasi assoluto silenzio della stampa nazionale, impegnata a inseguire le solite notizie di politica nostrana e gossip (da una ricerca in internet, solo uno dei quattro maggiori quotidiani italiani ha riportato un articolo dedicato alla notizia; recentemente “L’Espresso” la elencava tra le “4 novità destinate a cambiare il mondo, ma ignorate dai giornali”). Eppure la conclusione positiva dello studio è veramente importante sia sul fronte strettamente scientifico che su quello generale a sostegno del concetto, fortemente evaporato negli ultimi anni, che prevenire l’infezione da HIV si può. Innanzitutto con l’educazione comportamentale nell’incontro con un partner, omo o eterosessuale, poi con il profilattico, eventualmente con la circoncisione (che dimezza la probabilità di contrarre l’infezione per il maschio, non per la femmina) e, d’ora in poi, con un gel microbicida.
Veniamo alla novità scientifica (pubblicata da “Science”: Q. Abdool Karim, et al. Effectiveness and Safety of Tenofovir Gel, an Antiretroviral Microbicide, for the Prevention of HIV Infection in Women. Science 329, 1168, 2010). Il contesto è quello della prevenzione, lo stesso terreno del vaccino anti-HIV, che ha finora collezionato una lunga fila d’insuccessi più o meno clamorosi (anche se l’anno scorso è arrivato il primo risultato parzialmente positivo con lo studio RV144 condotto in Tailandia su 16.000 persone sieronegative).
Il concetto di microbicida anti-HIV nasce poco più di dieci anni fa stimolato proprio dall’incapacità d’individuare un vaccino efficace comprendendo qualsiasi agente in grado di prevenire o limitare l’infezione da HIV trasmessa per via mucosale (principalmente per via vaginale, ma potenzialmente anche rettale), con l’ovvia clausola della non tossicità ed assenza di effetti collaterali. Uno slogan di qualche anno fa definiva i microbicidi – qualora avessero funzionato - “the power of her” a sottolineare come in Africa ed in altre parti del mondo la donna spesso non sia nelle condizioni d’imporre al partner l’uso del profilattico. Il primo studio clinico in merito – giusto dieci anni orsono - fu un fallimento in quanto il candidato microbicida nonossinolo-9 (uno spermicida largamente utilizzato a scopo anti-concezionale) non solo non ha protetto dall’infezione da HIV, ma l’ha addirittura favorita rispetto al gruppo controllo che ha applicato un gel placebo. Si è poi capito che il nonossinolo-9 causa esfoliazione epiteliale ed infiammazione, pabulum ideale per la replicazione del virus nelle cellule immunitarie CD4+ (linfociti T, macrofagi e cellule dendritiche) richiamate in loco da segnali chemiotattici.
Da allora, si sono succeduti diversi studi sostenuti da enti pubblici, quali la Commissione Europea (progetti EMPRO, EUROPRISE ed il recente CHAARM), e privati, quali la Bill & Melinda Gates Foundation (Bill Gates ha definito i microbicidi la tappa intermedia verso il vaccino). Nei primi anni ci si è concentrati su molecole quali zuccheri complessi, chemochine modificate ed anticorpi anti-HIV, miranti ad impedire l’interazione delle cellule bersaglio col virus (che, oltre al recettore primario CD4, deve interagire col co-recettore chemochinico CCR5 per riuscire ad infettarle). Queste molecole hanno prodotto risultati interessanti ma, complessivamente si sono dimostrate troppo deboli e/o poco specifiche per prevenire l’infezione in vivo. Perciò, dopo l’ultimo recente fallimento in fase III del polisaccaride PRO2000, si è concluso che difficilmente questa categoria di molecole avrebbe dimostrato efficacia clinica.
Va qui sottolineata la difficoltà di studiare i potenziali microbicidi in vivo, ovvero la mancanza di qualsiasi surrogato clinico (o bio-marcatore) che possa predirne l’efficacia o meno. Infatti, per un farmaco è possibile testare l’effetto sull’abbattimento della viremia o sul recupero di linfociti T CD4+ circolanti e di un vaccino si può almeno quantificarne l’immunogenicità e lo spettro di risposte immunitarie indotte. Non così per un microbicida per cui, in passato, si sono considerati l’incidenza di altre infezioni sessualmente trasmesse e la presenza di marcatori d’infiammazione a livello mucosale, fattori troppo indiretti per essere affidabili indicatori d’efficacia. Non rimane quindi che affidarsi, dopo gli opportuni studi in vitro e l’utilizzo di primati non umani infettati dal SIV (parente stretto di HIV), ad uno studio clinico ben disegnato soprattutto per quanto riguarda la capacità di monitorare l’utilizzo o meno del microbicida.
E’ quello che ha fatto CAPRISA 004, uno studio interamente Sud-Africano (altro successo per questa nazione, mentre ospitava i mondiali di calcio! CAPRISA è infatti l’acronimo di “Centre for the AIDS Programme of Research in South Africa”) guidato dalla coppia Quarraisha e Salim Abdool-Karim. La molecola attiva, Tenofovir, aveva già dimostrato ottime caratteristiche per essere sviluppato a microbicida, quali efficacia nella prevenzione della trasmissione virale da madre a figlio, lunga emivita e protezione dalla trasmissione vaginale di SIV in macache. Lo studio CAPRISA 004 prevedeva una prima applicazione del gel non oltre 12 ore prima del rapporto sessuale e una seconda appena possibile dopo lo stesso entro12 ore. Lo studio (in doppio cieco randomizzato ed inclusivo di placebo) è stato disegnato per donne HIV negative che avevano dichiarato almeno 2 rapporti sessuali negli ultimi 30 giorni. In totale, sono state arruolate 889 donne: 445 hanno ricevuto il gel contenente tenofovir 1%, 444 il placebo; i due gruppi erano omogenei per età, tipologia e frequenza di attività sessuale ed hanno ricevuto le stesse raccomandazioni su come prevenire l’infezione, inclusive dell’uso di un profilattico.
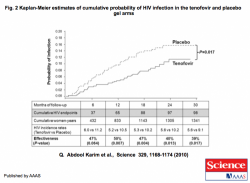
I risultati sono stati “clear-cut”: 38 infezioni nel braccio con tenofovir contro 60 nel braccio placebo (p=0.007) per un “incidence rate ratio” di 0.61 (95% CI 0.40-0.94) con una diminuita efficacia dopo 30 mesi (p=0.017) ed una migliore aderenza allo studio in coloro che rimanevano sieronegative dopo 30 mesi (54% di protezione per coloro con >80% aderenza rispetto al 39% complessivo e del 28% per coloro che hanno utilizzato il gel una volta su due – vedi la figura); l’aderenza complessiva allo studio, misurata recuperando gli applicatori del gel, è stata di ca. il 75%. L’uso del gel a base di tenofovir non ha avuto alcun impatto sui livelli di viremia plasmatica in quelle donne che si sono infettate (un caveat per l’utilizzo di farmaci quali microbicidi è la possibilità che inducano selezione di ceppi virali resistenti) mentre le concentrazioni di tenofovir nel fluido cervico-vaginale erano correlate significativamente all’efficacia preventiva.
Un valore aggiunto – anche a livello di conoscenza di base! – è stato l’analisi retrospettiva sulla potenziale efficacia di tenofovir gel sull’infezione da herpes simplex 2 (HSV-2) a livello genitale (altra malattia sessualmente trasmessa: le infezioni sessuali viaggiano in gruppo! Secondo UNAIDS, ca. il 20% degli adulti sessualmente attivi ne sono affetti in modo asintomatico in assenza di una terapia efficace). Il razionale era costituito dal fatto che tenofovir è strutturalmente simile al farmaco anti-erpetico cidofovir. Dell’intera coorte, 443 donne sono state considerate a rischio d’infezione da HSV-2. Il gel a base di tenofovir ha dimostrato anche in contro l’infezione erpetica un’efficacia del 51%: 29 casi nel braccio ricevente il gel col farmaco rispetto a 58 nel braccio placebo (IRR: 0.49, p=0.003). Nelle donne che hanno applicato il tenofovir gel non si sono registrati casi di resistenza farmacologica o di effetti collaterali, pericoli per la gravidanza o cambiamenti comportamentali implicanti un maggior rischio di contrarre l’infezione.
CAPRISA 004 è, ovviamente, solo il primo passo, ma rappresenterà la pietra miliare degli studi futuri che dovranno dimostrare efficacia almeno equivalente o altri vantaggi rispetto al gel a base di tenofovir. Il successo, ancorché parziale, dell’approccio microbicida offre l’opportunità di poter affrontare il problema della diffusione dell’infezione da HIV in queste zone sfortunate del mondo (ma anche in Italia, dove la propagazione del virus è ripresa anche e soprattutto tra i più giovani a seguito della non-/dis-informazione sull’argomento) con un’arma in più. Il modellista matematico Brian Williams – dello stesso team Sudafricano – ha calcolato che l’uso di questo gel potrebbe prevenire oltre un milione d’infezioni e 800.000 morti da AIDS nei prossimi 20 anni.
Standing ovation!