Ipotizzando che gli infetti sviluppino un’immunità persistente all’infezione, i due autori confrontano due scenari basandosi sull’andamento dell’epidemia in Piemonte. Il primo scenario ipotizza una rilassamento rapido delle misure entro fine maggio; il secondo una permanenza ridotta del distanziamento sociale combinato con un efficace tracciamento dei casi. Risultato: nel primo caso ci si attende un secondo picco dell’epidemia verso metà agosto, con un numero di ricoveri in terapia intensiva simile alla prima ondata, con il 70% della popolazione immune a fine anno. Nel secondo caso un picco epidemico minore ma prolungato nel tempo, con la fine dell'epidemia non prima di maggio 2021.
Nell'immagine, "Quarantine loading", di Sofia Carra.
L’emergenza Covid-19 ha visto il Governo e le Regioni mettere in atto provvedimenti di salute pubblica eccezionali che hanno comportato forti restrizioni delle libertà personali ed un impatto negativo sulle attività economiche e sul reddito. Tali provvedimenti, che per loro natura sono emergenziali e quindi di durata limitata nel tempo, sono stati accettati dalla quasi totalità della popolazione italiana in base ad un principio di solidarietà sociale.
Le misure di distanziamento sociale imposte alla popolazione hanno sicuramente contribuito a ridurre temporaneamente la circolazione di SARS-CoV-2, come pare evidente dall’andamento favorevole dei diversi indicatori epidemiologici e sanitari utilizzati per seguire l’andamento del contagio. Da tali indicatori appare anche chiaro l’andamento sfasato dell’epidemia tra le diverse regioni italiane. Tuttavia, solo un grado di immunità collettiva (la cosiddetta immunità “di gregge”, ossia la protezione offerta dai soggetti immuni a quelli suscettibili) sufficientemente elevato può interrompere persistentemente la circolazione del virus nella popolazione. Tale immunità si può ottenere attraverso l’introduzione (con copertura adeguata della popolazione) di un vaccino efficace e lo sviluppo di immunità naturale in risposta all’infezione.
Tuttavia, un vaccino efficace al momento non è disponibile e non lo sarà per molti mesi a venire, anche a fronte dell’attività di ricerca di numerosi istituti e del tentativo di introdurre disegni di studio più celeri per i trial (Callaway, 2020). Dunque SARS-CoV-2 continuerà a circolare nella popolazione fintanto che la quota di soggetti suscettibili nella popolazione non scenderà al di sotto di una soglia critica, che si può calcolare utilizzando il tasso di riproduzione dell’epidemia in fase iniziale (R0). La circolazione del virus nella popolazione potrebbe poi essere influenzata da variazioni stagionali, come è già stato osservato nel caso di altri coronavirus; al momento però non ci sono dati sufficienti per sapere come si comporterà COVID-19. Quindi, assumendo che i soggetti guariti dall’infezione sviluppino un’immunità protettiva rispetto ad una reinfezione, è fondamentale quantificare, e se possibile controllare, la velocità con cui l’immunità collettiva si costituisce nella popolazione italiana. In linea di principio si deve rallentare il contagio senza bloccarlo in modo tale da mitigare l’impatto della malattia sulle strutture sanitarie e tuttavia ridurre significativamente la frazione di soggetti suscettibili nella popolazione.
Per misurare la velocità dell’immunità collettiva è necessario condurre degli studi epidemiologici di sieroprevalenza ripetuti su campioni rappresentativi della popolazione, mentre per controllare la velocità di diffusione dell’infezione è importante limitare i contatti tra i casi contagiosi ed i soggetti suscettibili. In fase epidemica iniziale ed in fase di eliminazione, l’identificazione dei casi infetti ad il tracciamento dei loro contatti è una misura indispensabile per il controllo della trasmissione di un’infezione. Questa strategia serve a rendere più efficienti ed efficaci le procedure di isolamento: infatti solo i soggetti infetti, sintomatici o meno, sono messi in quarantena per due settimane, mentre i loro contatti stretti vengono a loro volta sottoposti al test per verificare che non siano stati infettati.
Inoltre, partendo dall'esperienza, in negativo, di Lombardia e Piemonte, andrebbero evitate in modo assoluto le occasioni di assembramento come manifestazioni, concerti, raduni sportivi che costituirono occasione di innesco importante, rendendo impossibile, qualora fosse stata tentata, qualsiasi azione di tracciamento dei contatti. Altresì, attenzione particolare andrebbe posta nella protezione delle comunità confinate, specialmente se costituite da soggetti anziani.
Le diverse istituzioni dovrebbero quindi concentrarsi come minimo sui seguenti 3 punti:
- mantenere un adeguato numero di posti letto nelle terapie intensive del paese per fare fronte ad una probabile seconda ondata epidemica;
- condurre indagini epidemiologiche di siero-prevalenza ripetute per quantificare la velocità con cui l’epidemia evolve e con cui l’immunità collettiva si viene a costituire (assumendo che la risposta anticorpale conferisca un’immunità persistente nei confronti di una reinfezione da SARS-CoV-2);
- rafforzare e coordinare il sistema di tracciamento dei casi ed i loro contatti.
Al fine di illustrare questi tre punti abbiamo stimato il tasso netto di riproduzione dell’epidemia (Rt) in base ai dati piemontesi (figura 1) e utilizzato un modello matematico di trasmissione del SARS-CoV-2 per confrontare tra loro due scenari epidemici (figura 2) basandoci sull’andamento dell’epidemia di SARS-CoV-2 in Piemonte.
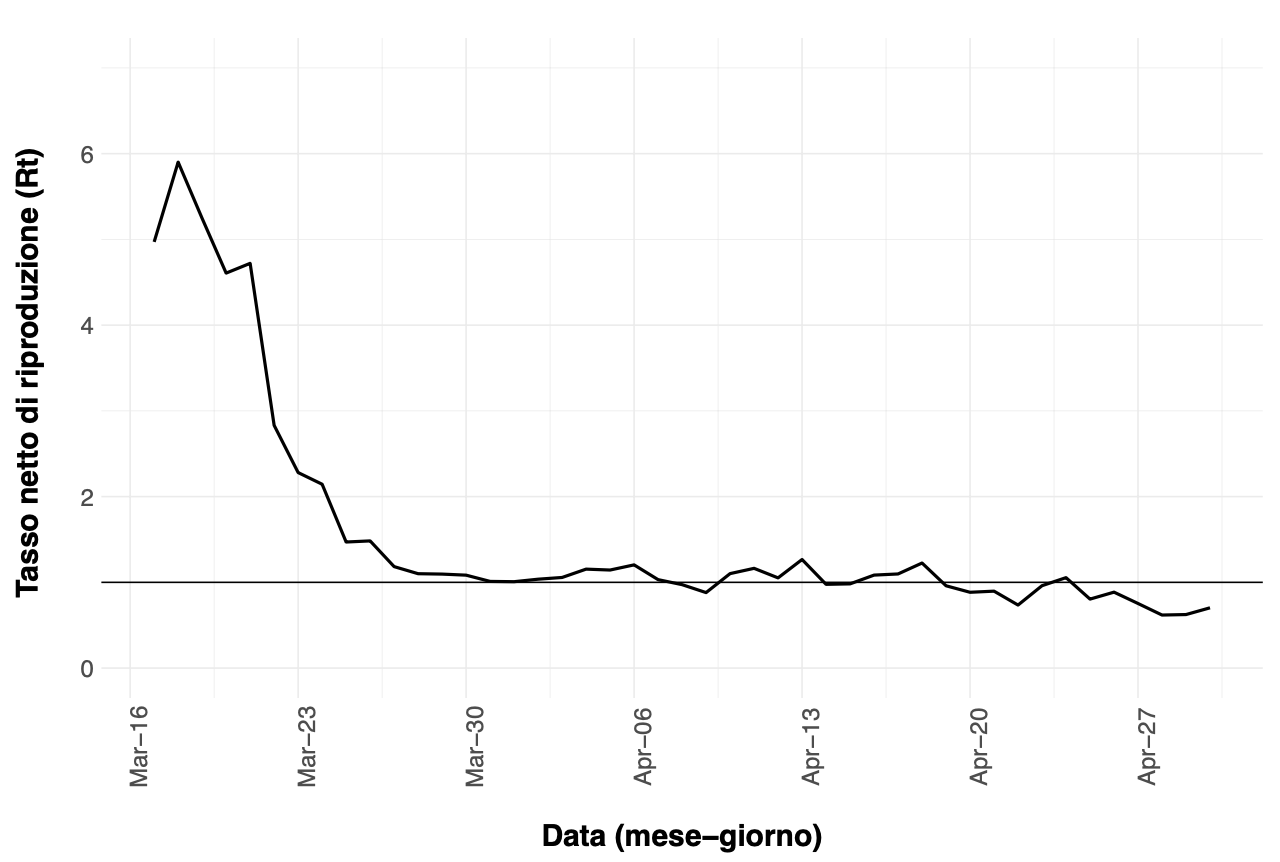
Figura 1. Andamento temporale del tasso netto di riproduzione dell’epidemia (Rt) dal 10 marzo 2020 al 1° Maggio 2020. La linea orizzontale rappresenta la soglia critica di Rt = 1.
È importante sottolineare che il modello utilizzato per le simulazioni, come la quasi totalità dei modelli pubblicati, assume che i soggetti infetti sviluppino un’immunità persistente all’infezione. I dettagli metodologici del modello sono descritti nel box metodologico.
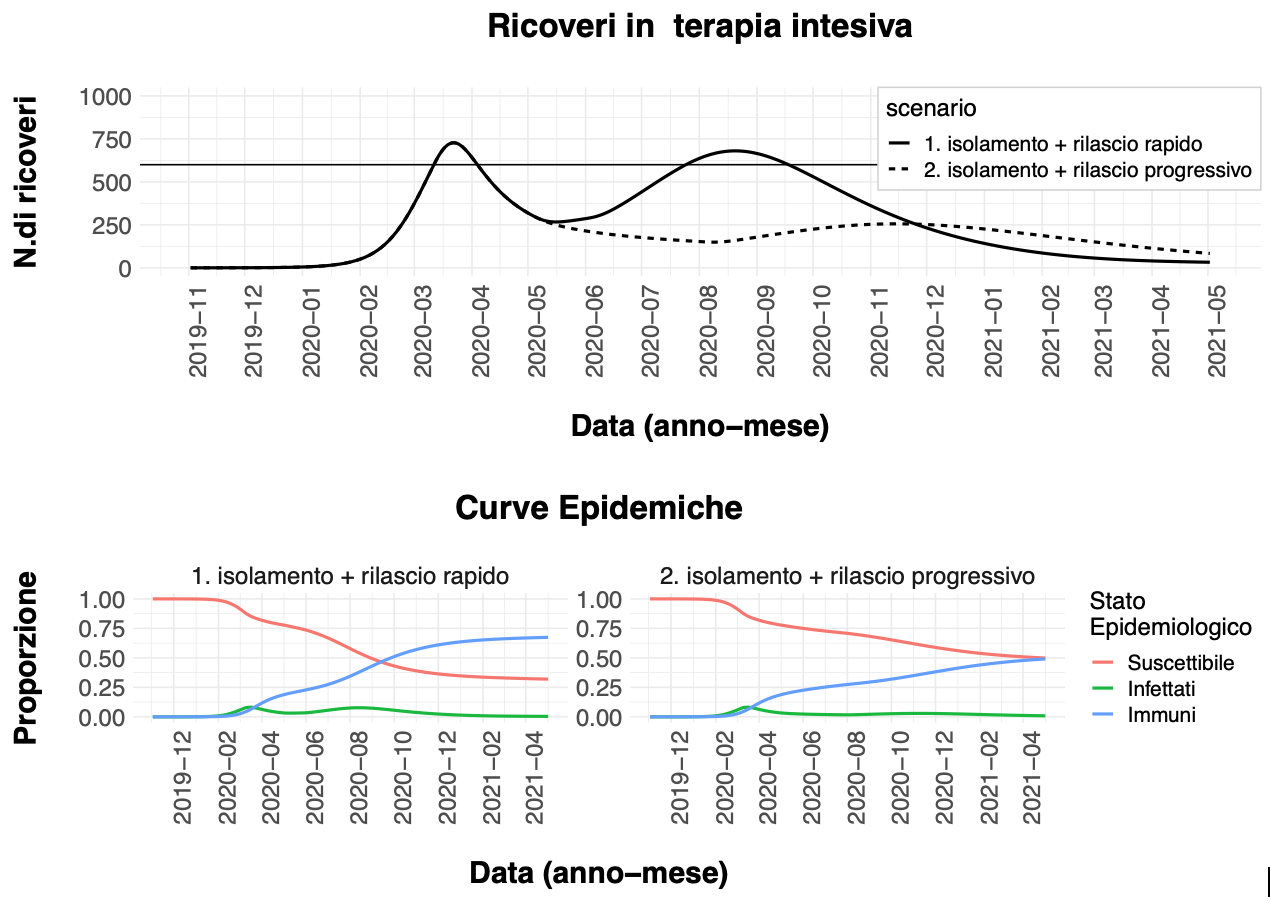
Figura 2. Scenari epidemici simulati. Il riquadro superiore mostra i casi ricoverati in terapia intensiva predetti dal modello in caso di un rilascio rapido delle misure di distanziamento sociale (curva continua); ed in caso di un rilascio progressivo combinato con tracciamento e poi isolamento efficace dei casi potenzialmente contagiosi (curva discontinua). La soglia di disponibilità dei posti letto in terapia intensiva è fissata a 600 (dato Protezione Civile rilevato a metà aprile). I riquadri inferiori rappresentano la dinamica temporale dell’epidemia corrispondente ai due scenari simulati. A sinistra sono rappresentati le frazioni di soggetti suscettibili (curva rossa), infetti (curva verde) ed immuni (curva blu) nel caso di un rilascio rapido delle misure di distanziamento. A destra invece è rappresentato il caso di un rilascio progressivo combinato con un efficace tracciamento ed isolamento dei casi potenzialmente contagiosi.
Il primo scenario simulato (figura 2, curva continua nel riquadro superiore e riquadro inferiore sinistro) assume che le misure di distanziamento sociale che hanno condotto alla riduzione di Rt vengano rapidamente rilassate entro fine maggio per ritornare ad un’intensità di contatti sociali paragonabile a quella di febbraio; mentre il secondo scenario (figura 2, curva discontinua nel riquadro superiore e riquadro inferiore destro) assume una permanenza seppur ridotta del distanziamento sociale combinato con un’efficace azione di tracciamento dei casi e quindi una riduzione dei contatti potenzialmente contagiosi fino ad agosto 2020. Le due curve si sovrappongono nel corso della prima ondata epidemica.
Nel primo caso (curva continua) ci si attende un secondo picco dell’epidemia verso metà agosto, con un numero di soggetti ricoverati in terapia intensiva comparabile a quelli osservati nel corso della prima ondata. In questo caso si raggiungerebbe una quota di immuni di circa il 70% della popolazione a fine anno.
Nel secondo caso invece (curva discontinua) il secondo picco epidemico è significativamente ridotto di intensità ma prolungato nel tempo, con un’estinzione epidemica prevista non prima di maggio 2021. In questo caso il numero massimo di soggetti ricoverati in terapia intensiva sarà anche esso ridotto.
I riquadri inferiori della figura 2 illustrano la dinamica del contagio sotteso alle due curve di ricoveri in terapia intensiva. A sinistra (scenario con rilascio “rapido” delle misure di distanziamento sociale), si vede che la curva dei soggetti immuni (curva blu) cresce rapidamente nella popolazione, mentre a destra (scenario con controllo dei contatti potenzialmente contagiosi), la stessa curva cresce più lentamente e il numero dei soggetti suscettibili (curva rossa) decresce altrettanto lentamente.
Appendice Metodologica
Il tasso netto di riproduzione dell’epidemia (Rt) è stato calcolato utilizzando i dati ottenuti dal sito della Protezione Civile (https://github.com/pcm-dpc/COVID-19), in cui è riportato il totale giornaliero dei casi confermati a partire dal 24 febbraio 2020. Al fine di tenere conto della periodicità della segnalazione dei casi che risente del ciclo lavorativo settimanale abbiamo utilizzato una media mobile su cinque giorni includendo il valore del giorno stesso e quelli dei due giorni precedenti e successivi. Utilizzando i valori ottenuti abbiamo poi calcolato il rapporto fra il numero di casi in uno specifico giorno e quelli presenti da 4 fino a 10 giorni precedenti. Rt è stato ottenuto come media di questi rapporti. Considerata l’incompletezza e l’instabilità dei dati abbiamo utilizzato le informazioni disponibili a partire da metà marzo. Anche altri autori, con metodi simili, raggiungono risultati paragonabili (Riccardo et al. 2020).
Il modello matematico di trasmissione è stato sviluppato modificando quello proposto da Anderson R et al (2020). Si tratta di un modello deterministico, non stratificato per fasce di età, con struttura SEIR in cui i soggetti possono trovarsi i 4 stati epidemiologici: suscettibili (S), in incubazione - infetti ma non contagiosi (E), infetti e contagiosi (I) e immuni (R). La transizione tra i diversi stati è regolata da specifici tassi di transizione che dipendono dalla durata media di ogni stato (Baussano et al, 2010). Ad ogni istante di tempo t Il tasso di infezione di un soggetto suscettibile dipende dal tasso di riproduzione dell’epidemia in fase iniziale (R0), dalla durata dello stato infettivo e dalla frazione di soggetti infetti nella popolazione allo stesso istante. Una frazione dei soggetti infetti può essere ricoverata ed una frazione di questi può essere trasferita in terapia intensiva. Infine, i soggetti ricoverati in terapia intensiva e quelli ospedalizzati sono soggetti ad uno specifico tasso di mortalità. In tabella sono riportate le distribuzioni utilizzate per parametrizzare il modello, che è stato programmato utilizzando il Package “EpiModel” - CRAN - R Project (Jennes et al., 2018). Le stime qui riportate corrispondono al valore medio ottenuto da 100 simulazioni campionando lo spazio dei parametri riportato in tabella. La variabilità delle stime non è stata presentata nella figura per non distrarre il lettore dal messaggio che qui si voleva dare. Tuttavia, lo script del modello consente di calcolare la variabilità delle stime. Lo script del modello è disponibile su richiesta presso gli autori dell’articolo.
Tabella. Parametri utilizzati per ottenere le proiezioni.
Bibliografia
Anderson RM et al., 2020 How will country-based mitigation measures influence the course of the COVID-19 epidemic? Lancet. https://doi.org/10.1016/S0140-6736(20)30567-5
Baussano I et al., 2010. Modelli matematici della trasmissione delle infezioni. Epidemiol Prev.
Callaway E. Scores of coronavirus vaccines are in competition — how will scientists choose the best? Nature, doi: 10.1038/d41586-020-01247-2.
Jenness SM et al., 2018. EpiModel: An R Package for Mathematical Modeling of Infectious Disease over Networks. Journal of Statistical Software. http://doi.org/10.18637/jss.v084.i08
Lavezzo E. et al., 2020. Suppression of COVID-19 outbreak in the municipality of Vo, Italy. MedRvix. https://doi.org/10.1101/2020.04.17.20053157
Riccardo F et al., 2020. Epidemiological characteristics of COVID-19 cases in Italy and estimates of the reproductive numbers one month into the epidemic. MedRxiv https://doi.org/10.1101/2020.04.08.20056861
Conflitti di interessi. Nessuno.
Esonero di responsabilità. Laddove gli autori sono identificati come personale dell’Agenzia Internazionale per la Ricerca sul Cancro / Organizzazione Mondiale della Sanità, gli autori sono i soli responsabili delle opinioni espresse in questo articolo e non rappresentano necessariamente le decisioni, le politiche o le opinioni dell'Agenzia Internazionale per la Ricerca su Cancro / Organizzazione Mondiale della Sanità.
Ringraziamenti. Gli autori ringraziano Damien Georges (IARC) per il suo contributo allo sviluppo del modello e Rodolfo Saracci per le riflessioni che hanno stimolato la stesura dell’articolo.

