Dall'ossitocina alle gemelline cinesi
- 8258 letture

Crediti: MaxPixel. Licenza: CC0 Public Domain
Cosa accomuna un ormone noto da moltissimo tempo e le piccole Lula e Nana, nate in Cina qualche mese fa? Una cosa semplice e a un tempo inaspettata, che proietta tutto in una dimensione di enorme valenza potenziale: la possibilità di controllare e influenzare i nostri comportamenti sociali e cognitivi.
Cominciamo con il piccolo ormone chiamato ossitocina: è prodotta dai nuclei ipotalamici del cervello e secreta dalla porzione posteriore dell’ipofisi. E’ stata isolata quasi 70 anni fa e caratterizzata come l’ormone che avvia le contrazioni uterine durante il parto e promuove la contrazione dei dotti lattiferi della mammella e quindi la secrezione del latte. Per decenni, l’ossitocina è stata confinata a questi due compiti ma, in tempi più recenti, studi sia sugli animali che sull'essere umano ne hanno inaspettatamente ampliato lo spettro dell’attività, aggiungendovi effetti del tutto slegati dal fenomeno parto-lattazione, attinenti alla sfera sessuale e, specialmente, sociale. Così si è visto che i livelli di ossitocina aumentano durante l’orgasmo sessuale, ma anche durante manifestazioni affettive. Numerosi studi comportamentali hanno dimostrato che la sua somministrazione favorisce comportamenti di generosità nei riguardi del prossimo e riduce comportamenti di rigetto xenofobico o comunque legati a differenze etniche e culturali: e così sono fiorite definizioni fantasiose dell’ossitocina completamente dimentiche della sua funzione originaria nel parto e nella lattazione. L’ossitocina è ora divenuta "l’ormone della generosità", "dell’altruismo" o addirittura "dell’amore".
Il sogno -o l’incubo- insito nella possibilità di modificare a volontà il comportamento dell’uomo e le sue emozioni, che già era già stato grossolanamente inseguito attraverso la via chirurgica o elettrostimolatoria, si è così prepotentemente riaffacciato, stavolta usando la via chimica.
Il caso delle gemelline cinesi riguarda un ambito scientifico molto diverso e più direttamente legato ad aspetti molecolari: più precisamente, alla rivoluzionaria e importantissima nuova tecnologia genetica definita dall’acronimo CRISPR. In soldoni, e semplificando all’estremo, questa tecnologia consente di compiere operazioni di editing del genoma, usando “forbici” molecolari che tagliano il DNA dovunque si desideri, rimuovendo così, o inattivando, geni: ad esempio eleminandone porzioni o introducendovi mutazioni inattivanti. E, come è evidente, l’operazione di editing compiuta sulle cellule germinali trasmetterà la modificazione alle generazioni successive.
Entrando in medias res, l’embrione che ha dato origine alle gemelline è stato modificando introducendo una delezione inattivante di circa 30 basi nel gene CCR5, che codifica il ricettore per una chemochina indispensabile al virus HIV per penetrare nelle cellule che intende invadere. He Jiankui, il ricercatore cinese responsabile dell’esperimento, voleva evidentemente rendere le gemelline inattaccabili da HIV: voleva, per così dire, immunizzarle geneticamente contro il virus.
Raccontata così, la storia non dovrebbe suscitare reazioni negative, anzi. Se non forse quelle legate alla sua irreversibilità e alla trasmissione dell’editing del genoma alla progenie. Obiezioni peraltro non sostanziali di fronte all’ovvio vantaggio di eliminare malattie ereditarie da sempre flagello dell’umanità o, come in questo caso, di rendere la progenie immune a malattie sicuramente devastanti come l’AIDS.
Il problema, qui, è un altro: la splendida tecnologia CRISPR, forse uno dei più importanti contributi della storia della scienza, è ancora giovane: del genoma ora si sa molto, ma non ancora abbastanza. Perché i geni non sono elementi isolati che agiscono in un limbo privo di interazioni reciproche, e a un gene, vale a dire al suo prodotto proteico, può corrispondere più di una funzione. Detto in modo sbrigativo, all’editing di un gene possono seguire effetti collaterali inaspettati che saranno, per forza di cose, irreversibili: ovvio quindi che occorra procedere con cautela, molta cautela, nel maneggiare l’editing del genoma. Peraltro, va sottolineato come questi effetti collaterali imprevisti (e ce lo insegna la biologia dei sistemi complessi) dipendano dallo specifico make-up genetico dell’individuo, vale a dire dalla sequenza di molti altri geni, che può ripresentarsi in forme diverse. Diviene quindi difficile, se non impossibile, prevedere tali effetti su base generale, dato che dipendono dalla natura del genoma di ogni singolo individuo. Ed è qui che - chiedendo venia per la metafora irriverente- è cascato l’asino del ricercatore cinese.
L’asino in questo caso è stata una ricerca sui topi condotta da un folto gruppo di ricercatori statunitensi, inglesi, giapponesi e coreani, che ha dimostrato, in modo impeccabile ma del tutto inaspettato, che il gene CCR5 non si limita, come era ben noto, a influenzare l’effetto di una chemochina ma ha anche un profondo effetto repressore sui parametri sperimentali comunemente usati per studiare la cognizione e la memoria. Inattivandolo, si rendono i topi della ricerca, per dirlo in modo colloquiale, più intelligenti. Ergo, pur con tutte le cautele necessarie quando si trasmettono all’uomo risultati ottenuti su animali, è del tutto ragionevole aspettarsi che il futuro cognitivo delle due gemelline sia, per così dire, particolarmente radioso.
L’articolo sui topi è apparso nel 2016, presumibilmente quando il ricercatore cinese stava iniziando a lavorare al progetto delle gemelline: era a quel punto al corrente del lavoro sui topi? In altre parole, lo motivava solamente il problema di HIV o già aveva pensato a possibili effetti cognitivi? Su questo non vi sono state sinora risposte convincenti, che andrebbero naturalmente al di là dell’interesse particolare del ricercatore. Perché non occorre particolare fantasia per immaginare il polverone generale che questi risultati provocheranno: si incominciano del resto già a vederne le prime inevitabili avvisaglie. Ed è facile prevedere che il frastuono supererà quello provocato dalle ricerche sull’ossitocina, che pure hanno aperto la sdrucciolevole strada del controllo scientifico dei comportamenti e, più in generale, delle capacità cerebrali umane. Perché qui non si tratta di studi comportamentali, qui si parla di molecole e di geni: e all’orizzonte già si addensano nubi intellettuali, morali, giuridiche. Probabilmente anche politiche, ed è giusto paventarne il rischio: perché il controllo di quelle che sono comunemente intese come le capacità superiori dell’essere umano, già forse possibili con interventi ormonali -ossitocina docet- può ora essere dietro l’angolo. Un’efficiente eugenetica, duole dirlo, è ora un’opzione realmente praticabile.
Ma una cosa occorre dire al riguardo con tutta la possibile chiarezza: non deve essere possibile avventurarsi oltre queste metaforiche Colonne d’Ercole senza avere prima ottenuto una maggiore e approfondita comprensione di cosa significhi l’introduzione nel genoma di variazioni che abbiano lo scopo di modificare la nostra vita psichica.
CRISPR e le gemelle cinesi: rigore, please
- 7257 letture

He Jiankui durante il secondo Summit internazionale sull’editing del genoma umano (Crediti: 湯惠芸/Wikimedia Commons. Licenza: pubblico dominio)
“Le forbici molecolari tagliano il DNA dovunque volete” scrivono Carafoli e Bucci. Sì, è proprio così: si possono rimuovere o inattivare geni, eliminare porzioni, o introdurne altre. E non c’è nessuna ragione, secondo me, per non ricorrere al gene editing se questo davvero sapesse eliminare tante tare ereditarie dalla faccia della Terra. Però, quando uno si mette a farlo, scopre che le cose sono molto più complesse e in fondo prima di discutere se lo si debba fare o no, gli scienziati – che poi siamo tutti noi – dovrebbero porsi il problema di saperlo fare, e di saperlo fare bene. Insomma, dobbiamo assicurarci che quello che vorremmo fare riusciamo a farlo davvero, senza creare problemi magari più gravi della malattia che vorremmo guarire.
Il caso delle gemelline cinesi è emblematico e allora vediamo che cosa sono riusciti a fare davvero He Jiankui e i suoi colleghi rispetto a quello che avrebbero voluto fare. L’idea dei ricercatori cinesi era (sembra) quella di proteggere le gemelline dal virus dell’HIV eliminando 32 paia di basi nel gene CCR5 tramite la tecnologia CRISPR. Però in una delle due gemelline, Lulu, uno dei due alleli è rimasto inalterato (da quello che si è capito dai risultati presentati da He Jiankui al meeting di Hong Kong per il secondo Summit internazionale sull’editing del genoma umano); nell’altro allele c’è stata davvero una delezione e proprio del gene CCR5, ma solo di 15 paia di basi. Questo basta a disattivare il gene? Forse no. E’ verosimile che si crei una proteina molto vicina a quella normale che potrebbe pure funzionare.
Invece Nana, l’altra gemellina, non ha avuto una delezione delle 32 basi in nessuno dei due alleli. Quello che è successo davvero è che in un allele si è inserita una base e nell’altro se ne sono perse 4. E sapete perché? Perché la tecnica usata da He Jiankui si basa su quello che in termine tecnico si definisce non-homologous end joining: vuol dire che dopo il taglio del DNA, indotto dalla famosa forbice molecolare, si possono introdurre praticamente a caso inserzioni o delezioni proprio nel momento in cui il DNA si richiude.
E allora? A dirla tutta siamo al punto di prima. Non è successo quello che avrebbero voluto e non sappiamo nemmeno di sicuro quali saranno le conseguenze di quello che hanno fatto. Chissà… Ma queste varianti bloccheranno in futuro l’ingresso del virus dell’HIV nelle cellule delle gemelline? Forse sì, ma non è nemmeno detto che sia davvero così. E la questione della memoria e dell’intelligenza? Anche lei è legata al gene CCR5, che non solo governa l’ingresso del virus dell’HIV nelle cellule ma è un inibitore naturale delle sinapsi fra neuroni nell’ippocampo (la regione del cervello che ci aiuta a ricordare). Se fossero riusciti a fare davvero quello che volevano, è possibile che un giorno le gemelline Lulu e Nana avranno più memoria e saranno più intelligenti degli altri bambini, proprio come i topi cui si toglie CCR5, che hanno più memoria e sembrano essere più intelligenti degli altri.
E allora? Un piccolo insegnamento dagli “esperimenti” di He Jiankui senza nessuna pretesa: la scienza va avanti ed è un gran bene che sia così. Ma mentre i filosofi e i bioetici discutono su ciò che sia giusto o non giusto fare, noi dobbiamo sempre restare fedeli a tre principi: rigore, rigore e rigore, please.
CRISPR, più ricerca e meno moratorie
- 8477 letture

Crediti: fernandozhminaicela/Pixabay. Licenza: Pixabay License
…encore un effort si vous voulez être républicains!
(de Sade)
Premesso che mi convincerò dell’esistenza delle due bambine geneticamente editate tramite CRISPR solo quando saranno viste e controllate da un team di ricercatori indipendenti, si può stare al gioco e accettare, per il piacere di discutere, i dati forniti volontariamente da He Jankui, come ipotetico caso di studio. L’intervento di Bucci e Carafoli solleva la questione dell'affidabilità dei dati scientifici discussi pubblicamente e delle controversie disinfornate che si possono generare. Se il caso fosse vero, l’esperimento solleverebbe diverse questioni, di cui tre sono a mio giudizio le più interessanti:
- lasciando da parte il consenso informato, perché ci troviamo in Cina dove questa procedura risulta piuttosto estranea alla mentalità collettivista prevalente, la questione più generale è se, ammesso che vi fosse il consenso dei genitori, fosse moralmente lecito fare un esperimento su embrioni umani, introducendo modifiche anche nella linea germinale;
- come si inquadra il fatto che lo sperimentatore non sia stato preciso nell’uso del sistema enzimatico di taglio, modifica e rammendo del DNA;
- cosa possono fare i ricercatori per evitare che venga introdotto qualche divieto irragionevole alla ricerca, ovvero se ha senso una moratoria volontaristica lanciata da alcune delle migliori teste della biomedicina occidentale, ma non firmata e criticata sempre da alcune delle migliori teste della biomedicina occidentali
La questione di cui al primo punto è stata a più riprese discussa nel secolo scorso da qualche scienziato, da qualche divulgatore o da qualche scrittore, ed è diventata un tema seriamente analizzato agli inizi degli anni Settanta; poi ancora nei dintorni del 1990, quando è stata effettuato il primo intervento clinicamente controllato ed eticamente approvato di terapia genica: fu stabilito, a larga maggioranza e mai più messo in discussione, che sulla linea germinale non si deve intervenire. Noi non avremmo il diritto di interferire con il caso e la selezione naturale, cioè con la “naturale” determinazione del pool genico della future generazioni.
Le perplessità ragionevoli riguardavano il fatto che molti geni malattia sono stati selezionati dagli agenti infettivi perché davano un vantaggio agli eterozigoti. Sarebbe stupido privare le future generazioni di geni che sono patogeni in omozigosi ma proteggono l’eterozigote (ma se il gene drive eliminasse le zanzare vettrici di malaria, perché no?). Inoltre, alcune varianti del gene potrebbero codificare per proteine diverse a seguito dei rimaneggiamenti (splicing), con effetti diversi sul fenotipo, di tipo polifunzionale. Infatti, il gene CCR5 (modificato da He) è polifunzionale, perché implicato nella resistenza ai virus HIV e anche in modifiche che interessano aree del cervello correlate con la memoria a breve termine e l’apprendimento.
Non penso si debba considerare eccezionale o intoccabile la linea germinale, rispetto a quella somatica. Nella misura in cui si conosceranno le funzioni dei geni, vi saranno le prove – intendo solide indicazioni dopo sperimentazioni su animali – che gli effetti “collaterali” non saranno dannosi e l’impatto a livello popolazione rimane inesistente, si dovrebbe consentire l’intervento sulla linea germinale umana.
L’argomento per cui mancherebbe il consenso dei nascituri è debole, perché oggi i genitori non chiedono il consenso ai nascituri quando decidono di far nascere un bambino pur sapendo che sarà gravemente malato. Ricordo le discussioni sui donatori di midollo programmati, dove si è visto che i bambini messi al mondo per usare il midollo o il cordone ombelicale non sono stati trattati come un mezzo, ma anch’essi come un fine (Kant).
La questione di cui al secondo punto dipende dal fatto che non sono state sviluppate delle linee guida internazionalmente negoziate su come procedere nell’editare il genoma umano. Tutti riconoscono che He ha commesso errori, ed è fuori discussione che la competenza e l’etica nella good clinical pratice sono inseparabili. Gli errori sono probabilmente anche la conseguenza del fatto che non poteva chiedere supporto a ricercatori più bravi né far circolare l’informazione sull’esperimento – che di sicuro però era noto al Ministero della Salute cinese, dove He pare fosse di casa. È chiaro che il nostro è stato un pasticcione, ma questa è una conseguenza anche del clima esageratamente di sospetto e moralista che nel mondo occidentale interessa la ricerca biomedica, a causa di cambiamenti culturali e tragici misfatti. Non vorrei essere tacciato di blasfemia, ma noi celebriamo Pasteur, Koch, Behring, e molti altri in quanto eroi della medicina, ma gli esperimenti imprecisi, ovvero temerari e in diversi casi mortali, che effettuarono su soggetti umani, li consegnerebbero oggi al carcere per molti anni. Non sto relativizzando.
Perché la moratoria sull'uso dell'editing genetico (CRISPR) è inutile e dannosa
La questione di cui al punto tre si presterebbe a una lunga discussione etico-sociologica. Penso che la moratoria chiesta da Lander&Co sia un atto un po’ irresponsabile. Come lo fu la moratoria che nel 1973 portò alla conferenza di Asilomar sul DNA ricombinante. E suona quasi beffarda la firma sull’ultima del novantaduenne Paul Berg, che era primo firmatario della moratoria del 1973. Quella moratoria e la conferenza che si concluse con la tesi che non esisteva un bio-rischio accertabile e che bastava fare regole stringenti per l’uso del DNA ricombinante ebbe l’effetto di scatenare, comunque, la tecnofobia sociale e politica contro le biotecnologie. I biologi molecolari pensano ancora che fosse un segno di responsabilità – moratoria più conferenza e dichiarazione tranquillizzante dei massimi esperti – ma fu letto come una presa in giro da una parte dell’opinione pubblica, che applicando la disposizione umana al complottismo immaginò malafede e conflitto di interesse dei ricercatori. Joshua Leberberg (ma anche James Watson che non aveva ancora manifestato le debolezze senili di questi anni) si rese conto dell’errore, e presagì le ricadute dannose per la scienza. Si potrebbe anche ricordare quel che accadde, a proposito di moratorie, quando nacque Dolly.
Alla luce di questi precedenti, anche la moratoria sull’uso dell’editing genomico per fare modifiche ereditarie su embrioni umani è sbagliata oltre che inutile, visto che non ha nessuna forza giuridica o sanzionatoria reale. Michele de Luca ha scritto, al contrario, che il caso cinese deve portare i laboratori occidentali che usano questa tecnica a fare più ricerca su embrioni umani, senza farli nascere, e che sarebbe dannoso mettere in mano ai governi qualche pretesto per vietare la ricerca su embrioni umani. Come De Luca, anche Church, Dealy, Doudna e vari altri non hanno aderito alla moratoria.
Gli scienziati davvero responsabili non dovrebbero chiedere una moratoria, che a livello di singoli cittadini o scienziati non ha alcun senso, ma dovrebbero chiedere di fare più ricerca perché è l’unico modo efficace per disincentivare smanettamenti pericolosi nei Paesi non democratici e non liberali. L’Occidente ha le migliori regole e i più efficaci controlli per evitare abusi. È vero che ne accadono ugualmente, ma suona paradossale che chi sta messo meglio come regole ed etica della scienza invochi una moratoria. La dovrebbero nel caso chiedere i cinesi, se proprio volessero garantirsi il tempo di raggiungere la maturità scientifica e l’etica occidentale.
Editing genomico: maneggiare con cura
- 8212 letture

Crediti: Elias Sch./Pixabay. Licenza: Pixabay License
Qualche settimana fa, su questa rubrica abbiamo pensato di discutere l’annuncio fatto dal ricercatore cinese He Jankui di aver editato embrioni umani mediante la tecnica CRISPR e, più in generale, la possibilità di alterare genoma, comportamento e capacità dell’essere umano. Dopo la nostra introduzione, sono intervenuti i professori Remuzzi, Corbellini e Panzica per offrire i loro punti di vista; e le svariate migliaia di letture che la nostra introduzione e i loro contributi hanno raccolto testimoniano il vivo interesse che questi temi hanno per il pubblico. Crediamo sia giunto il momento di chiudere (almeno temporaneamente) questa interessante discussione con alcune considerazioni finali.
Abbandonare la pretesa di una moratoria assoluta
Partiamo da una questione generale, in linea con quanto scritto da Corbellini: le moratorie e le barriere etiche autoimposte non servono a impedire che ciò che è scientificamente realizzabile prima o poi sia realizzato da qualcuno. L’etica prescrittiva è un prodotto della cultura e del modo di vedere di alcuni gruppi in un determinato momento storico, ed è ben difficile che riesca a essere riconosciuta come universalmente valida; figuriamoci in un settore come quello della ricerca scientifica, in cui si tendono a riconoscere come vincolanti solo i limiti della nostra immaginazione e dei nostri metodi, e dove è facile contrapporre ai valori morali prodotti in un certo contesto – per esempio quello delle élite culturali che attualmente governano l’Occidente – altri valori e altri modi di intendere il progresso dell’umanità, quali quelli di stampo collettivista di una nazione-mondo come la Cina.
Naturalmente, queste osservazioni di carattere generale, molto ben sottolineate da Corbellini, non proibiscono affatto di considerare invece analiticamente le conseguenze e i dilemmi etici del caso specifico delle gemelline cinesi. In altre parole, se abbandoniamo la pretesa di basare una moratoria assoluta su un’etica generica e di pretese universalistiche, possiamo dedicarci con maggiore serenità a valutare i dubbi e le implicazioni sul piano morale dello specifico modo di agire di He Jankui. Possiamo, per esempio, domandarci: cosa ha fatto, in realtà? Aveva dichiarato di aver verificato che la delezione introdotta nel gene CCR5 delle gemelline fosse quella nota come Delta32, ma di fatto non sappiamo ancora come siano stati effettuati questi controlli; come ha scritto Remuzzi, pare invece accertato che la delezione delle 32 coppie di basi non sia proprio avvenuta.
Mentire o rappresentare artatamente i propri risultati nella ricerca scientifica sono considerati entrambi peccati gravi: e tanto più lo sarebbero nel caso specifico in cui si sta parlando di interventi su esseri umani. Non sappiamo, però, se nell’affermazione del ricercatore cinese vi sia dolo o se si tratti semplicemente di incompetenza professionale. Di quello, cioè, che nel gergo scientifico si definisce normalmente sloppyness. Diamo quindi a He Jankui, che non sembra essere un biologo molecolare di prima grandezza e attendibilità, il beneficio del dubbio. Ha più volte dichiarato che una seconda gravidanza è in corso: che ne è stato? Chi sta seguendone gli sviluppi, dove sono i dati, dove sono i protocolli applicati? In Cina si è estesa una cortina sul caso, aumentando di fatto le incertezze non solo scientifiche, ma anche etiche, su quanto è stato fatto originariamente, ma anche su quanto si sta facendo tuttora.
Considerazioni sulla scelta dell'editing a CCR5
Queste sono riflessioni generali sull’esperimento di He Jankui. Ma sono altre questioni più specifiche che riguardano la particolare scelta di editare il gene CCR5. Perché vi sono dubbi sulle vere ragioni della scelta. Sapeva il ricercatore cinese dei possibili effetti cognitivi degli interventi sul gene CCR5? Lo ha sempre negato, ma i risultati sulla cognizione esistevano in letteratura dal 2016, cioè da quando lui ha disegnato il suo protocollo e ha iniziato il lavoro. Ed era già comunque noto, e quindi probabilmente lo era anche a lui, che gli interventi di editing genetico possono, per dire così, sfuggire di mano, e introdurre mutazioni e delezioni al di fuori di quelle che si vogliono produrre.
Cosa del resto che non dovrebbe stupire, e che rimanda a quello che avevamo scritto nella nostra introduzione di qualche settimana fa: il genoma è qualcosa di molto complesso, in cui le interazioni reciproche si sprecano, e in cui i singoli geni non vivono in un metaforico limbo individuale. Non si è ad esempio visto proprio poche settimane fa che la delezione Delta 32 nel gene CCR5, quella appunto che He Jankui voleva introdurre in omozigosi, ha effetti sulla durata della vita (che pare esser minore nei portatori della delezione Deta 32), legati verosimilmente all'aumentata suscettibilità a diverse malattie infettive, come ad esempio l’influenza? E a parte gli effetti cognitivi, non sono forse stati documentati anche inaspettati effetti positivi della delezione, quali quelli sul miglioramento degli effetti dannosi dell’ictus cerebrale?
Tutto questo va ricordato perché l’editing genetico e questo tipo di lavoro in generale, giriamola come vogliamo, portano direttamente sulla strada dell’eugenetica. E il biologo molecolare cinese questa strada l’ha imboccata alla garibaldina, senza valutare a priori tutti gli effetti delle mutazioni che voleva introdurre, che d’altronde al momento in nessun modo avrebbe potuto prevedere. E qui occorre fare un discorso chiaro: l’editing genetico, come ha scritto Remuzzi, non è di per sé cosa da far inorridire: occorre dirlo, chiaro e forte, perché c’è nell’aria il chiaro pericolo che si passi automaticamente ad una sorta di “reductio ad hitlerum”, finendo per buttare il bambino con l’acqua sporca. Addirittura, per continuare la metafora, per buttarlo con l’acqua pulita.
È sintomatico, ad esempio, che una delle co-inventrici, assieme a Emanuelle Charpentier e Virginjus Siksnys, della tecnica CRISPR-Cas9 che ha provocato la recente esplosione universale di interesse per il gene editing, abbia raccontato di un recente sogno - che a me, chiedo scusa, è parso inventato- in cui le era apparso Adolf Hitler… Perché, fantasie su Hitler a parte, la possibilità di modificare geni, eugenetica o no, in linea di principio è tecnologia di enorme importanza potenziale per la medicina: basti pensare alla correzione dei difetti dei geni responsabili per devastanti, e molto comuni, malattie genetiche. E non solo per la medicina: consente infatti di superare i bandi ancora messi in atto in molti Paesi nei confronti degli OGM in agricoltura.
Lavorare e ancora lavorare
Per concludere: il polverone internazionale suscitato dagli interventi sul gene CCR5 ha posto l’accento sulle questioni etiche, e non solo etiche, che ne stanno a monte. Come detto, moratorie o regolamenti repressivi di portata generale sull’utilizzo di tecnologie promettenti quali la tecnologia CRISPR sulle linee germinali umane -esperienza insegna- non saranno però efficaci: se qualcosa è scientificamente realizzabile, prima o poi qualcuno la realizzerà. Occorrerà, con molta umiltà e molta pazienza, lavorare, lavorare, e ancora lavorare sul genoma per comprenderne appieno il funzionamento. Solo dopo si potrà passare alla pratica, tenendo sempre presente che, probabilmente, a effetti inaspettati saranno pur sempre in agguato.
Un ultimo breve commento sul gene CCR5. È possibile che la sua scelta sia stata particolarmente sfortunata? Sì, è possibile. Ma ha avuto quantomeno il merito di porre gli specialisti di fronte alla necessità di confrontarsi con un problema molto più grande del CCR5, problema che è facile prevedere occuperà la scienza per un lungo tempo a venire. Sfortunata, però, la scelta di occuparsi del, gene CCR5 lo è stata anche per un motivo più spicciolo. La mutazione Delta 32 aveva lo scopo di inattivare il gene CCR5, impedendogli di mediare l’ingresso del virus HIV nelle cellule. Esistono però da anni già numerosi composti farmacologici che agiscono con efficacia sul ricettore CCR5, inattivandolo: a che pro, quindi, darsi da fare per introdurre nel gene CCR5 la delezione Delta 32?
Ossitocina e vasopressina, nuovi orizzonti per vecchi ormoni
- 32022 letture

Nella puntata “Dall'ossitocina alle gemelline cinesi” della rubrica Vero o Falso abbiamo parlato di come la tecnologia CRISPR che He Jiankui sostiene di aver impiegato per modificare il genoma di due neonate possa, attraverso le modifiche al gene CCR5, avere un effetto sui parametri sperimentali comunemente usati per studiare la cognizione e la memoria. Sulla base di questa considerazione, i precedenti articoli della puntata (“CRISPR e le gemelle cinesi: rigore, please” e “CRISPR, più ricerca e meno moratorie”) hanno analizzato gli aspetti etici e scientifici dell'esperimento di Jiankui e delle sue conseguenze nella comunità dei ricercatori. Ma il tema della manipolazione del comportamento è affiorato con forza anche a seguito degli studi condotti sull'ossitocina, che avevano portato a definirla l'ormone “dell'altruismo” o addirittura “dell'amore”. Proprio in seguito all’interesse riscontrato per i temi inerenti alla manipolazione del comportamento mediante interventi di vario tipo, e in particolare per quanto riguarda le possibilità offerte dalla chimica e dalla farmacologia, abbiamo chiesto a Giancarlo Panzica, esperto nella fisiologia ormonale dell’ossitocina, di scrivere un compendio della migliore conoscenza disponibile sul tema. Il risultato è la breve, accurata e completa review che vi presentiamo, in cui ci sembra di poter sottolineare soprattutto l’emergenza nella discussione di un secondo ormone, la vasopressina, di cui sin qui si è discusso solo marginalmente, nel regolare antagonisticamente il sistema dell’ossitocina. L’importanza di considerare gli effetti di singole molecole nell’intero sistema d'interazioni molecolari non può essere sottaciuta; e per questo, giustissimo ci pare l’inserimento nella discussione almeno del principale antagonista dell’ossitocina. Buona lettura.
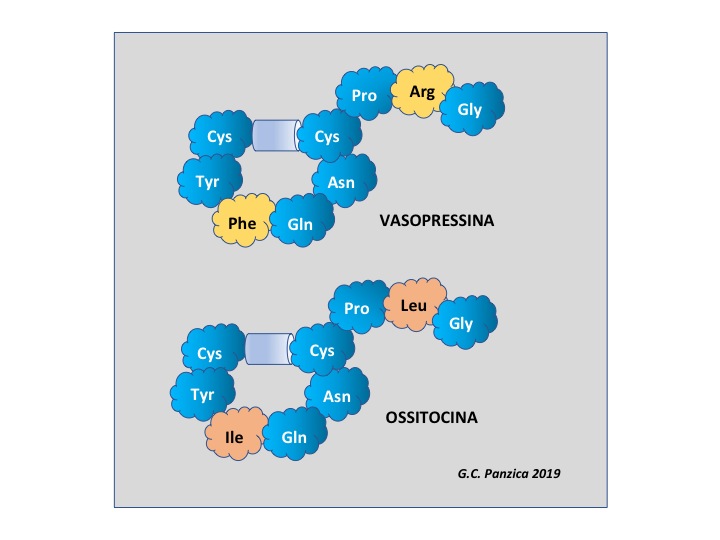
L’ossitocina e la vasopressina sono i primi ormoni di origine neuronale che siano stati identificati. Essi sono infatti prodotti da neuroni ipotalamici del nucleo sopraottico e paraventricolare che inviano i loro assoni alla neuroipofisi dove i due ormoni vengono rilasciati nella circolazione sanguigna. L’ossitocina facilita il parto e stimola la secrezione del latte, mentre la vasopressina è anche conosciuta come ormone antidiuretico e regola l’omeostasi idrico-salina dell’organismo.
Questi due ormoni non sono in grado di passare la barriera emato-encefalica e quindi per lungo tempo si è pensato che non potessero essere in grado di influenzare direttamente il tessuto cerebrale. Tuttavia, si è scoperto che i recettori per l’ossitocina e per la vasopressina sono presenti in molti nuclei cerebrali, suggerendo che questi peptidi abbiano altre funzioni nel sistema nervoso centrale. In parallelo, studi morfologici hanno chiarito che esistono anche altri gruppi di neuroni e fibre a vasopressina e ossitocina che non proiettano alla neuroipofisi, ma innervano diverse regioni nel telencefalo, nel diencefalo, nel tronco cerebrale, fino ad arrivare al midollo spinale1. Sembrerebbe quindi che esistano due pool di questi peptidi, uno, circolante nel sangue, per svolgere funzioni ormonali, l’altro, confinato nel sistema nervoso centrale, che può svolgere funzioni di regolazione dei circuiti nevosi.
Il ruolo nei comportamenti sociali e di coppia
In diversi modelli animali si è potuto verificare che ossitocina e vasopressina sono importanti per regolare i circuiti nervosi che controllano alcuni comportamenti sociali e di coppia. Molti studi sono stati condotti sulle arvicole di prateria, roditori che formano coppie stabili, che hanno comportamenti aggressivi verso gli intrusi e nei quali la cura della prole è affidata a entrambi i genitori. Si è dimostrato che il blocco del sistema a ossitocina determina una minor preferenza verso il partner abituale nella femmina, mentre il blocco del sistema a vasopressina opera allo stesso modo nel maschio. Questi effetti sono determinati dall’azione dei due peptidi su nuclei telencefalici diversi, ma appartenenti al cosiddetto circuito della ricompensa.
Un altro aspetto molto interessante è che la distribuzione del recettore della vasopressina nel circuito della ricompensa è diversa nei maschi di due specie di arvicole (di prateria e di montagna) che, pur essendo molto simili, hanno comportamenti di coppia opposti: le arvicole di montagna sono poligame, quelle di prateria monogame2. Se si fa esprimere il recettore della vasopressina delle arvicole di prateria nei maschi delle arvicole di montagna questi diventano monogami. In sostanza, una piccola mutazione nella struttura del recettore determina sia la sua diversa espressione sia un cambiamento radicale nel comportamento di coppia3.
Ossitocina, vasopressina e comportamento aggressivo
Altri studi hanno dimostrato che l'ossitocina e la vasopressina esercitano una notevole influenza anche sulla regolazione dello stress e dell’aggressività. In particolare, l'ossitocina induce la comparsa dell'aggressività materna (un meccanismo per difendere i piccoli dai pericoli esterni), mentre i topi maschi incapaci di produrre ossitocina hanno un aumento dei livelli di aggressività.
La vasopressina sembra avere genericamente un effetto di stimolazione del comportamento aggressivo, anche se sembra che questo effetto possa variare a seconda di specie, sesso ed esposizione a stimoli ambientali4. L'isolamento sociale aumenta i comportamenti aggressivi nei ratti e sembra associato a un aumento del numero dei recettori ipotalamici della vasopressina. Da questi esperimenti risulta quindi evidente che queste due molecole, conosciute per lungo tempo solo come ormoni neuroipofisari, hanno invece molteplici ruoli e regolano circuiti cerebrali importanti per il controllo di diversi comportamenti.
Gli studi sulle specie umana
Il passaggio dagli esperimenti sugli animali all’essere umano è sempre molto complesso e necessita di dati clinici e altre conferme; tuttavia, vi sono anche qui dei risultati particolarmente interessanti. Innanzitutto, vista l'incapacità della ossitocina e della vasopressina a passare la barriera emato-encefalica, la via di somministrazione è particolarmente critica e normalmente viene attuata una somministrazione intra-nasale, perché la mucosa olfattiva presenta dei neuroni in diretto contatto con l’ambiente esterno e quindi l’assorbimento delle molecole avviene in maniera semplificata. La somministrazione intra-nasale di ossitocina in volontari adulti sani sembra migliorare la percezione dei danni subiti in seguito ad aggressioni, ma non suscita il desiderio di rispondere all’aggressore. Inoltre, i livelli di ossitocina misurata nel liquor cerebrospinale mostrano una correlazione negativa con la propensione all’aggressività di pazienti che presentano disturbi della personalità.
Questi due dati sembrerebbero confermare l’idea che nella specie umana l’ossitocina riduca le reazioni aggressive e promuova comportamenti come la fiducia e la cooperazione. Come nei modelli animali, si pensa che la vasopressina abbia ruoli in contrasto con quelli della ossitocina: nel liquor cerebro spinale, ad esempio, i livelli di vasopressina aumentano in individui con abitudini aggressive. In sostanza, l’ossitocina avrebbe una azione anti-aggressività, mentre la vasopressina sarebbe pro-aggressività. Un recente lavoro sperimentale, con somministrazione intra-nasale di vasopressina e ossitocina, condotto in Olanda su un gruppo di 62 maschi di età compresa tra i 18 ed i 35 anni, ha confermato indicazioni in tal senso5.
Vista la distribuzione dei recettori per ossitocina e vasopressina nei nuclei che fanno parte del sistema della ricompensa, questi due peptidi sono considerati tra i maggiori candidati alla regolazione del cosiddetto “attaccamento”, ovvero dei legami che si stabiliscono in un contesto familiare (tra coniugi, con i figli, tra fratelli e sorelle) o in un contesto sociale più allargato (amici, scuola, ambiente di lavoro, animali di compagnia). In particolare, l’ossitocina sarebbe parte di un sistema dinamico che integra le risposte a livello cerebrale con quelle a livello del resto del corpo, e che consentirebbe l’espressione ottimale dei comportamenti sociali positivi che caratterizzano i legami di attaccamento6. Particolare importanza ha il riconoscimento visivo che determina una impennata nella produzione di ossitocina. Questo vale sia per il riconoscimento dei familiari (e in particolare dei figli), sia per i segnali visivi che si scambiano i cani con i loro padroni. In quest'ultimo caso si è potuto dimostrare che il picco di ossitocina avviene in entrambi i “partner” rafforzando l’attaccamento tra umano e cane7 (Nagasawa et al, 2015). Un meccanismo analogo servirebbe a stabilire il rapporto che si instaura tra madre e neonato, rafforzato da stimolazioni come quelle del capezzolo durante l’allattamento, da sensazioni olfattive (il classico odore del neonato) o uditive (il pianto), casi in cui la madre aumenta la secrezione di ossitocina.
L'ossitocina non agisce da sola e molti dei suoi effetti sono regolati dalle interazioni con la vasopressina, al punto che secondo molti autori entrambi questi peptidi possono essere considerati facenti parte dello stesso sistema, con azioni diverse ma complementari. Le funzioni di ossitocina e vasopressina dipendono dalla loro capacità di legarsi a una serie di recettori specifici presenti non solo nel circuito della ricompensa, ma anche nell’asse ipotalamo-ipofisi-surrene (l’asse neuroendocrino che controlla lo stress) e i centri encefalici che regolano il sistema nervoso autonomo (che controlla le risposte cosiddette involontarie degli organi interni del nostro corpo)6.
In un recente studio, condotto con la tecnica della risonanza magnetica funzionale (RMNf), i ricercatori hanno studiato coppie di novelli sposi sotto due aspetti: la misura dell’empatia verso il partner e la presenza di mutazioni nei recettori per l’ossitocina e la vasopressina. L’empatia, in studi come questi, viene misurata con la presentazione di fotografie del volto del partner, di amici o di sconosciuti con diverse espressioni facciali. È stato così dimostrato che quando il soggetto provava un forte senso di empatia verso la persona nella foto si attivavano le regioni appartenenti al circuito della ricompensa come l’amigdala e il pallido ventrale che, sono caratterizzate dalla presenza di un gran numero di recettori per l’ossitocina e la vasopressina. Inoltre, le persone che avevano mutazioni in questi recettori in grado di determinare una maggiore sensibilità ai due ormoni avevano risposte emotive più forti degli altri soggetti8.
Risposte complesse
In conclusione, il complesso degli studi condotti su modelli animali e sull’uomo sembra indicare che il comportamento sociale, con le sue risposte complesse, derivi da circuiti cerebrali presenti in tutti i mammiferi e le risposte alle singole situazioni dipenderebbero dalla stimolazione esterna, dall’espressione dei recettori per l’ossitocina e la vasopressina e dalla presenza di eventuali mutazioni di questi recettori. I comportamenti (e le malattie) che possono essere soggetti a questo tipo di controllo sono molteplici e vanno dalla aggressività, al comportamento di coppia, alla cura della prole, all’attaccamento agli animali domestici, alla depressione per arrivare fino alla schizofrenia e all’autismo. Ovviamente non tutto si può ridurre al dualismo ossitocina-vasopressina e molti altri fattori e neurotrasmettitori entrano in gioco nella regolazione di questi circuiti e comportamenti. Tuttavia la possibilità di intervenire proprio sulla ossitocina e la vasopressina con somministrazioni intra-nasali apre la possibilità ad interventi terapeutici non invasivi e di facile applicazione, insomma, per rifarmi all’articolo di Carafoli e Bucci, la possibilità di manipolare alcuni comportamenti sociali nell’uomo è una realtà di cui bisognerà tenere conto nel prossimo futuro.
Note
1. Fliers et al. (1988) Extrahypothalamic vasopressin and oxytocin in the human brain; presence of vasopressin cells in the bed nucleus of the stria terminalis. Brain Res. 375: 363-67
2. Young et al. (2011) The neurobiology of pair bonding: insights from a socially monogamous rodent. Front. Neuroendocrinology 32: 53-69
3. Lim et al. (2004) Enhanced partner preference in a promiscuous species by manipulating the expression of a single gene. Nature 429: 754-57
4. De Jong and Neumann (2018) Oxytocin and aggression. Curr Top Behav Neurosci 35:175-92
5. Berends et al. (2019) Oxytocin, vasopressin and trust: Associations with aggressive behavior in healthy young males. Physiol. Behav. 204: 180-85
6. Carter (2017) The role of oxytocin and vasopressin in attachment. Psychodynamic Psychiatry. 45: 499–518
7. Nagasawa et al. (2015) Social evolution. Oxytocin-gaze positive loop and the coevolution of human-dog bonds. Science 348: 333-36.
8. Acevedo et al. (2019) Beyond romance: Neural and genetic correlates of altruism in pair-bonds. Behav. Neurosci. 133: 18-31